黄宏龄团队发现KLF2在慢性病毒感染早期编程T细胞耗竭状态以限制抗病毒免疫的新机制
日期: 2026-04-28 访问数:2026年4月27日,厦门大学生命科学学院及翔安医院黄宏龄教授团队在Immunity上发表题为Krüppel-like factor 2 programs early exhausted T cell states and restrains antiviral immunity的研究论文,揭示了慢性病毒感染早期诱导T细胞耗竭程序、进而调控抗病毒免疫的新机制。

该研究首先建立了适用于慢性感染过程中T细胞命运分化的在体CRISPR筛选体系,结果表明转录因子KLF2对CX3CR1+效应耗竭亚群的分化至关重要。近年来,虽有研究指出T-bet、Batf等转录因子参与调控CX3CR1+细胞亚群的产生与维持,但过表达这些因子均无法将初始T细胞诱导分化为CX3CR1+状态。相比之下,KLF2的单因子过表达即可实现这一分化,凸显了KLF2在调控中的独特性和关键作用。
在功能层面,早期缺失KLF2可导致原本向CX3CR1+效应耗竭亚群分化的细胞重塑为CXCR6+终末耗竭状态,但这一转变并未伴随抗病毒功能的丧失。相反,KLF2的缺失促进了抗原特异性T细胞的累积,并增强了抗感染免疫。机制研究表明,KLF2缺失使T细胞的组织定位发生改变,使其迁移至树突状细胞富集区域,从而获得更强的增殖信号。进一步实验证实,阻断KLF2缺失引起的定位变化可逆转上述抗感染免疫增强效应。值得注意的是,KLF2缺失所导致的抗感染免疫增强并不伴随其他增效策略中常见的明显病理损伤,且该过程主要依赖于PD-1分子的上调。综上所述,这些发现为T细胞耗竭过程的生理意义提供了重要补充。
近期,多个独立研究团队相继报道KLF2除经典调控T细胞迁移外,在CX3CR1+ T细胞亚群命运决定中也发挥关键作用,相关成果发表于Science、Nature Immunology、《Immunity》《PNAS》等期刊,充分体现了该领域对这一生物学过程和科学发现的高度关注。
厦门大学黄宏龄教授为该论文唯一通讯作者。厦门大学生命科学学院博士研究生耿圣钧、李紫枫为论文共同第一作者,黄宏龄教授课题组多位成员参与研究。该工作得到了南京大学江亚军教授课题组、厦门大学、厦门医学院、厦门大学附属医院等多个合作团队的支持。研究获得国家重点研发计划、国家自然科学基金委、福建省杰出青年项目、厦门市自然科学基金、厦门大学南强A类人才计划、厦门大学生命科学学院汪德耀奖学金等资助。
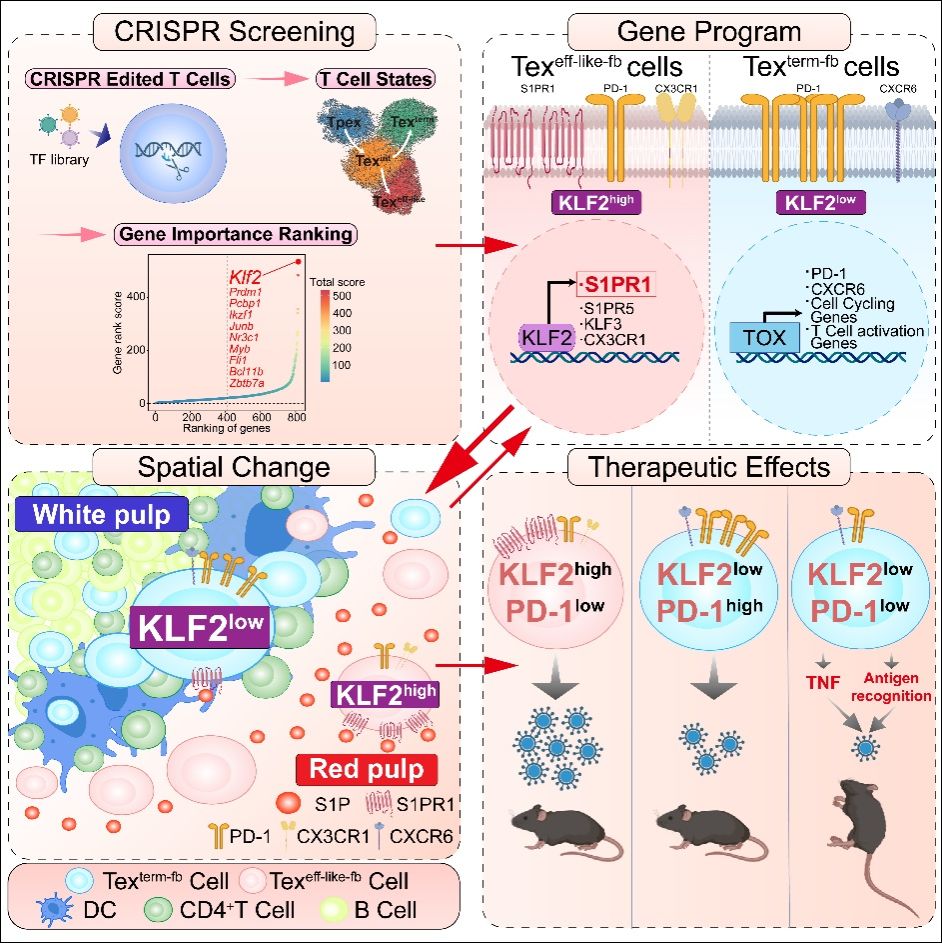
研究模式图
原文链接:https://www.sciencedirect.com/science/article/pii/S1074761326001408
(图/文 黄宏龄团队)
