揭祖亮团队揭示DYRK1A调控cDC1抗原交叉呈递及肿瘤免疫微环境的新机制
日期: 2026-04-28 访问数:树突状细胞(DCs)作为专业的抗原递呈细胞,在启动抗肿瘤免疫应答中发挥着不可或缺的作用。在各类DC亚群中,1型经典树突状细胞(cDC1s)凭借其卓越的交叉呈递肿瘤抗原及启动CD8⁺ T细胞的能力,成为抗肿瘤免疫的核心枢纽。然而,在肿瘤微环境中,肿瘤来源的代谢物及微环境信号常常抑制cDC1的功能,导致其抗原递呈受损并引发免疫耐受。因此,深入解析调控cDC1功能及其与肿瘤微环境互作的分子网络,对于优化癌症免疫治疗策略具有重要意义。
近日,揭祖亮团队、厦门大学附属第一医院李珣团队,联合河北大学附属医院史建红团队在《The Journal of Clinical Investigation》发表研究论文“DYRK1A enhances antitumor immunity in type 1 conventional dendritic cells via mTORC1 activation”。该研究鉴定了激酶DYRK1A在cDC1功能调控中的关键作用,并系统阐明了其分子机制及潜在的临床治疗意义。

该研究发现,在肿瘤微环境中,DYRK1A在肿瘤浸润DCs中呈高表达,其表达水平可被TLR配体、营养物质及T细胞来源信号(如IFN-γ)显著诱导。通过cDC1特异性敲除Dyrk1a小鼠模型,作者发现:DYRK1A缺失显著加速肿瘤生长,伴随肿瘤浸润CD8⁺ T细胞增殖受损、耗竭标志物(PD-1、TIM-3)上调及效应细胞因子分泌能力下降。转录组与流式细胞分析显示,DYRK1A缺失特异性下调cDC1表面MHC类分子及共刺激分子的表达,而对cDC2亚群无明显影响。进一步的抗原加工分析表明,DYRK1A缺失促进cDC1溶酶体生物发生与吞噬体酸化,导致外源抗原在溶酶体中被过度降解,从而严重削弱依赖蛋白酶体的抗原交叉呈递能力。
机制研究表明,DYRK1A通过调控TSC2-mTORC1信号轴促进cDC1的成熟与活化。DYRK1A可直接结合TSC2,并特异性磷酸化其Ser540位点。该磷酸化修饰增强了TSC2与E3泛素连接酶HUWE1的结合,诱导TSC2发生泛素化及蛋白酶体降解,从而解除其对mTORC1的抑制作用。遗传学实验表明,在Dyrk1a缺失的cDC1中同时敲除Tsc2,可完全恢复mTORC1的激活及cDC1的抗原呈递功能;而导入模拟磷酸化状态的TSC2突变体(S540D)则足以重塑cDC1的强效活化状态。上述结果证实,TSC2是该调控轴中的核心介导因子,而Ser540位点的磷酸化是维持mTORC1活性及cDC1功能的关键。
在功能层面,维持DYRK1A-TSC2轴活性可显著增强cDC1的抗肿瘤免疫反应。 在基于cDC1的过继细胞治疗模型中,Tsc2敲除成功挽救了DYRK1A缺失cDC1的免疫原性缺陷,恢复了肿瘤内效应T细胞的浸润及肿瘤控制能力。在人类多癌种(如黑色素瘤、膀胱癌、乳腺癌和肺癌等)TCGA及单细胞测序数据中,cDC1中DYRK1A的高表达与mTORC信号活化、效应T细胞富集特征及患者更优的总生存期呈显著正相关。上述结果提示,干预DYRK1A-TSC2信号轴具有潜在的临床转化价值。
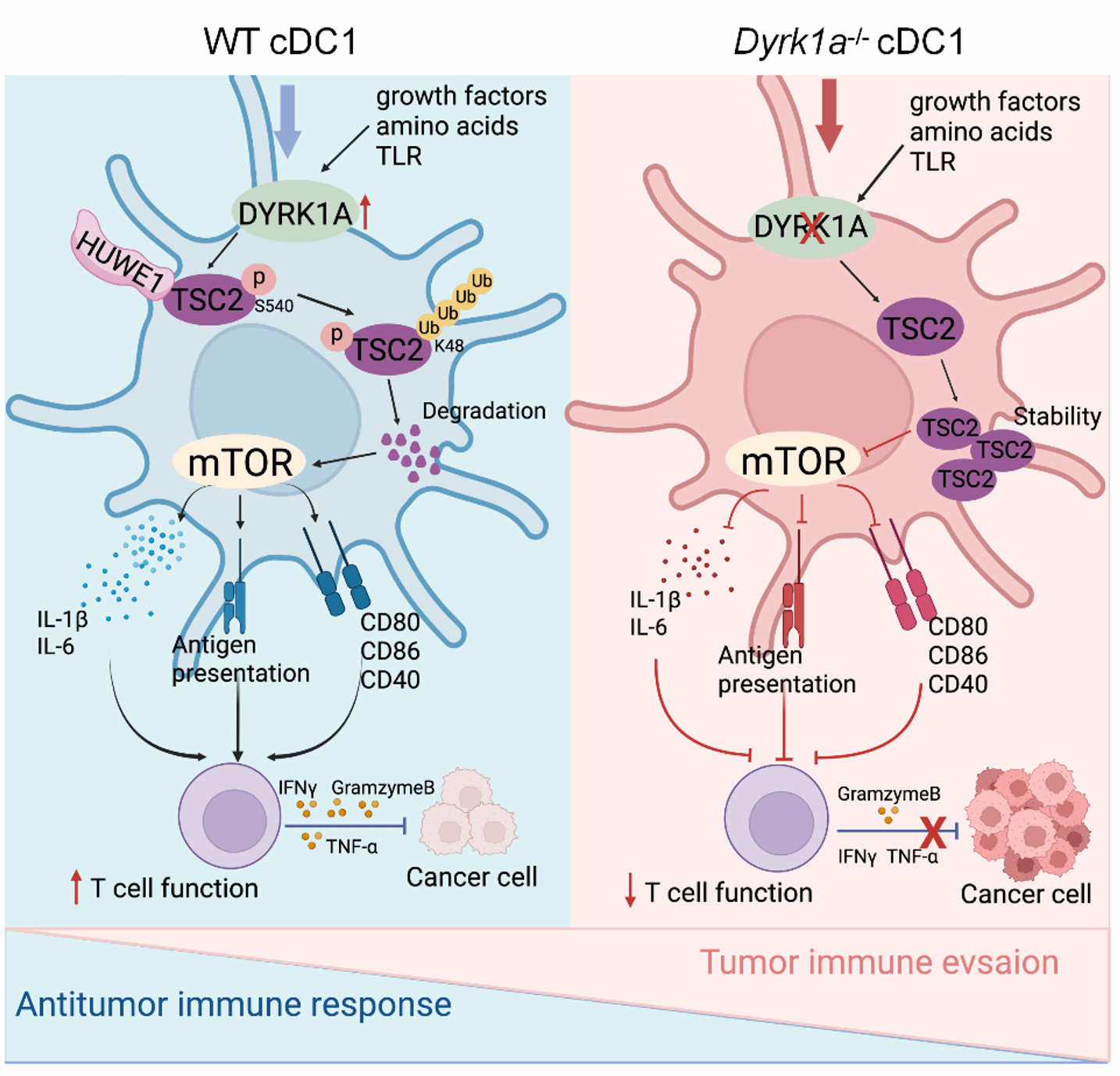
综上所述,该研究鉴定出1型经典树突状细胞抗肿瘤免疫新“开关”——DYRK1A。作为一种关键的微环境信号感受激酶,DYRK1A通过磷酸化促进TSC2降解,进而激活mTORC1信号通路,优化cDC1的抗原加工与交叉呈递功能,在抗肿瘤免疫中发挥核心调控作用。靶向激活DYRK1A或抑制TSC2功能,有望为提升DC疫苗及cDC1相关癌症免疫治疗的疗效提供新的策略。
厦门大学生命科学学院揭祖亮教授、厦门大学附属第一医院李珣副教授和河北大学附属医院史建红教授为本研究的共同通讯作者。厦门大学生命科学学院博士后王鸿姣、硕士研究生江赫、何松琳和厦门大学生命科学学院博士后任宋雯为本研究的共同第一作者,厦门大学公共卫生学院硕士研究生周春雲、厦门大学生命科学学院硕士研究生朱潘、本科生陈可人等为本研究做出了重要贡献。该研究获得国家高层次青年人才计划、国家重点研发计划、国家自然科学基金、厦门市重点医疗卫生项目、传染病疫苗研发全国重点实验室科研基金的资助。
原文链接:https://www.jci.org/articles/view/199108
(图/文 揭祖亮团队)
