张永有教授团队揭示遗传-营养互作在肝脏昼夜节律代谢调控中的核心作用
日期: 2025-08-27 访问数:昼夜节律是生物体适应日夜环境变化的重要生理机制。虽然核心时钟基因(如BMAL1、CLOCK等)在节律调控中起关键作用,但越来越多研究表明,非经典时钟基因调节因子以及遗传变异和环境因素(如饮食)在节律调控中同样至关重要。然而,这些因素如何协同作用,尤其在外周组织(如肝脏)中调控代谢节律,尚不明确。
2025年8月25日,我院张永有教授团队联合美国贝勒医学院(Baylor College of Medicine)管栋印团队在Cell Metabolism发表了题为Genetics-nutrition interactions control diurnal enhancer-promoter dynamics and liver lipid metabolism的研究论文。该研究发现,超过80%的肝脏节律性基因表达和染色质三维互作(enhancer-promoter interactions, E-PIs)受遗传与营养共同调控——这一比例远高于预期。换言之,个体的基因型决定了对不同饮食节奏的“敏感度”。

研究团队首先在人类和小鼠中发现,遗传变异(单核苷酸多态性,SNPs)可显著影响肝脏基因的昼夜表达模式。例如,脂滴形成关键基因PLIN2仅在携带特定基因型(AA型)的人群中呈现节律性表达,而在其他基因型人群中则无明显波动。这意味着若忽略遗传背景,许多节律基因在群体水平上易被“平均效应掩盖”,从而被忽视。
为深入探究其机制,团队选用两种遗传背景差异显著的小鼠品系(C57BL/6J 和 129S1/SvImJ),比较它们在正常饮食与高脂饮食条件下肝脏转录组、代谢物和三维基因组的动态变化。结果令人惊讶:绝大多数节律基因的表达模式高度依赖于“遗传背景 × 饮食”互作,而非仅由环境或遗传单一因素决定。
更引人注目的是,通过染色质互作分析(ChIA-PET),研究者发现雌激素相关受体γ(ESRRγ)作为一类非经典生物钟调控因子,在该互作机制中发挥核心作用。ESRRγ通过调控增强子-启动子的动态互作,影响脂代谢、尿素循环、氨基酸代谢等关键通路的时序性表达。
在人类脂肪肝样本中,团队进一步证实:与节律基因表达相关的遗传变异显著富集于增强子-启动子互作区域,并与血脂、胆固醇、载脂蛋白等代谢性状密切相关。这表明这些“节律SNP”不仅影响基因表达的时间模式,还可能直接参与代谢疾病的发病机制。
本研究首次系统揭示遗传-营养互作在肝脏昼夜节律代谢调控中的核心作用,并指出ESRRγ作为桥梁因子在该过程中的关键地位。这些发现不仅深化了对代谢疾病个体差异的理解,也为未来开展基于遗传背景的个性化时间干预策略(如择时饮食、择时用药)提供了科学依据。研究为我们理解个体差异在时间生物学中的作用提供了新视角,也解释了为何同是“8小时进食制”(TRE),有些人减肥效果显著,而有些人却无效——这可能源于基因型差异导致对进食时间响应不同。
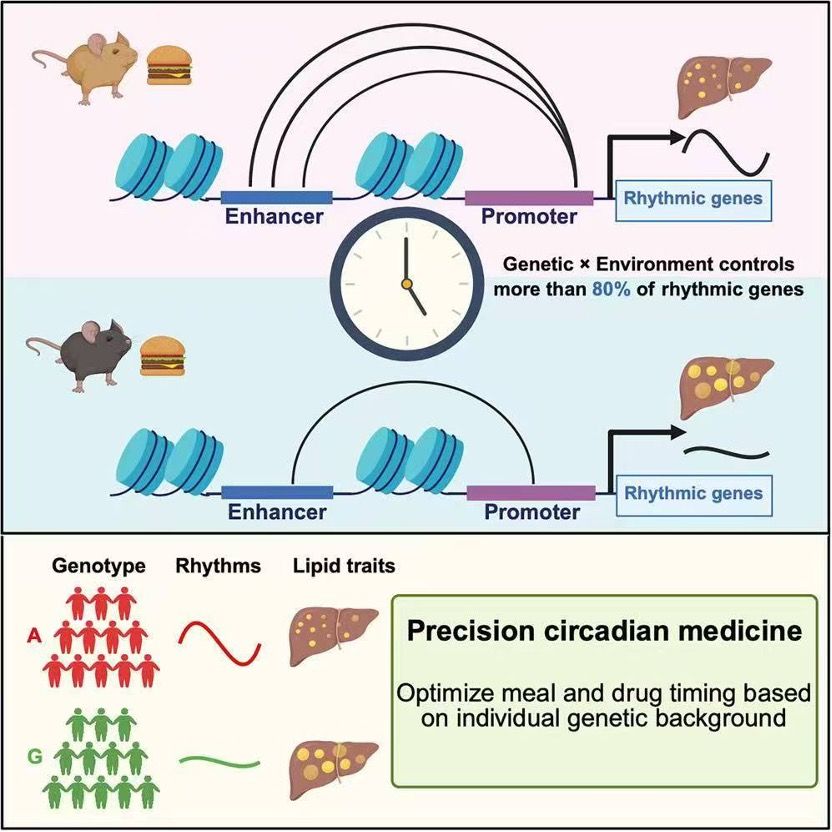
未来,我们或许不再笼统推荐“早吃好、晚吃少”,而是通过基因检测为每个人定制最合适的进食与用药时间表,真正实现“时间精准医学”(precision chronotherapy)。
厦门大学博士研究生周迪姝和美国贝勒医学院陈瑛博士为本文的共同第一作者。厦门大学张永有教授和美国贝勒医学院管栋印教授为本文的共同通讯作者。
【张永有教授团队简介】
张永有教授研究团队长期聚焦代谢调控及AI辅助蛋白设计与药物开发领域,重点开展肿瘤代谢调控、组织再生药物开发、分子工具酶开发、医学诊断试剂研制及AI辅助生物活性材料开发等研究,在Science、Cell Metabolism、Molecular Cell、PNAS、Redox Biology、Analytical Chemistry等期刊发表成果,相关研究获国家重点研发计划、国家自然科学基金及多项省市级项目支持。近五年申请专利15项,参与制定多项工具酶国家标准,并与生物医药科技企业联合攻关实现生物活性材料关键技术产业化;牵头组建校级和院级校企联合研发平台各1个,承担企业横向技术开发项目6项,实现技术开发合同金额累计超千万元。
原文链接:
https://www.cell.com/cell-metabolism/fulltext/S1550-4131(25)00356-0
(文/图 张永有教授团队)
