吴乔、陈航姿团队揭示肝星状细胞与肝癌细胞间形成反馈调控环促进肝癌进程的新机制
日期: 2026-03-13 访问数:肝细胞癌(Hepatocellular carcinoma, HCC)是全球范围内最常见肝恶性肿瘤,临床上超过80%肝癌发病由肝脏纤维化发展而来,提示肝脏纤维化与肝癌发生发展密切相关。肝纤维化的关键节点是肝星状细胞(Hepatic stellate cells, HSCs)的激活。健康肝脏中HSCs处于静息状态,细胞内富含维生素A脂滴;肝脏纤维化时,HSCs转为激活状态,细胞大量增殖,表现出α-平滑肌动蛋白(α-SMA)表达上调和胞外基质分泌增加等特点。近年来,肝星状细胞在肝癌进程中的作用受到广泛关注,但肝癌细胞与肝星状细胞间如何通过复杂互作网络调控肝癌进程,仍有许多关键问题尚待阐明。
2022年10月,吴乔、陈航姿团队在Nature Metabolism在线发表题为“HK1 from hepatic stellate cell-derived extracellular vesicles promotes progression of hepatocellular carcinoma”的研究论文。研究发现肝脏纤维化过程中,TGF-β1诱导HSCs中己糖激酶HK1发生棕榈酰化修饰,从而促进HK1通过胞外囊泡外泌;原本低表达HK1的肝癌细胞则劫持纤维化HSCs来源的胞外囊泡HK1,由此增强自身糖酵解能力并促进肝癌细胞增殖;此外,研究发现小分子化合物PDNPA通过靶向核受体Nur77阻断TGF-β1诱导的HK1外泌,进而抑制肝癌进程。该研究揭示了肝星状细胞来源的HK1重塑肝癌糖酵解代谢促进肝癌进程的新机制。然而,肝星状细胞来源的HK1是否发挥促肝癌糖酵解外的其他功能尚不清楚。
在前期研究基础上,团队进一步深入探索了肝癌细胞与肝星状细胞间复杂的互作网络。近日,该团队在Journal of Extracellular Vesicles在线发表题为“A Unique Intercellular Feedforward Loop From HK1 to TGF-β1 Promotes the Progression of Hepatocellular Carcinoma”的研究论文,揭示肝星状细胞来源的HK1和肝癌细胞来源的TGF-β1形成细胞间正反馈调控环,由此加剧肝脏纤维化和肝癌生长。

研究通过分析临床肝癌和正常肝脏组织单细胞测序数据发现:肝癌组织中,肝癌细胞葡萄糖代谢水平与肝星状细胞内TGF-β通路活性、HSCs激活程度显著正相关。实验证实:激活型HSCs通过胞外囊泡向肝癌细胞传递代谢酶HK1上调肝癌细胞内葡萄糖代谢,由此促进肝癌细胞分泌经典促纤维化因子TGF-β1,最终反馈调控HSCs激活及其外泌HK1。机制上,肝星状细胞来源的HK1通过上调肝癌细胞内己糖胺代谢通路促进肝癌细胞中蛋白N-糖基化修饰水平,其中,pro-TGF-β1蛋白第82、136和176位天冬氨酸会被诱导发生N-糖基化修饰,由此促进肝癌细胞分泌TGF-β1;分泌的TGF-β1进一步诱导静息状态HSCs转向激活型HSCs,由此反馈调控HSCs外泌HK1并加剧肝脏纤维化。临床肝癌组织空间转录组数据揭示,肝癌细胞和肝星状细胞间的互作与肝星状细胞活化程度密切相关;同时,临床肝癌组织芯片同样证实上述反馈调控环发生于肝癌进程,并与肝癌患者不良预后密切相关。
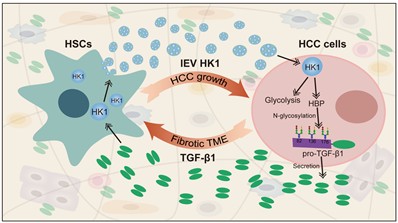
肝星状细胞与肝癌细胞间恶性反馈环示意图
综上,激活型HSCs外泌HK1与肝癌细胞分泌TGF-β1形成的正反馈环不仅加强了肿瘤细胞的代谢优势,同时还加剧纤维化的肝癌微环境,最终导致肝癌的恶性进展。以上研究为理解肝星状细胞与肝癌细胞间的复杂互作网络提供了新见解,同时为未来开发新的治疗策略提供了潜在靶点。
该论文的共同第一作者为博士后陈旗涛和黄巧玲,通讯作者为陈航姿教授。该工作获得国家自然科学基金联合基金项目、青年项目和博士后国资计划等资助。
原文链接:http://dx.doi.org/10.1002/jev2.70255
(图/文 吴乔、陈航姿团队)
