李勤喜教授和何伟玲教授团队揭示核蛋白Pirin通过正反馈调节ROS水平和炎症反应促进肝细胞癌发生的机理
日期: 2025-07-02 访问数:肝细胞癌(HCC)是一种常见且高致死性的肝癌,具有多因素复杂的致病机制。长期慢性炎症和活性氧(ROS)水平升高是其发病及进展的关键驱动因素。但长期以来,调控这一过程的关键分子机制尚未完全明确。
2025年6月27日,李勤喜教授、何伟玲教授团队在Gut杂志上在线发表题为Nuclear Pirin promotes HCC by acting as a key inflammation-facilitating factor的研究文章,首次揭示了核定位Pirin (PIR)在肝癌发生中的重要作用。

研究发现,HCC发展过程中,肝细胞内ROS水平的升高会引起氧化应激传感蛋白PIR的甲硫氨酸85和93位点发生氧化修饰,导致PIR从细胞质转运至细胞核。在核内,PIR作为转录辅助因子与关键转录因子RELA协同作用,激活NF-κB信号通路,促进炎性细胞因子(如TNFα和IL-6)的表达,炎性细胞因子进一步刺激ROS产生,由此形成的正反馈环路不仅加剧了肝脏的炎症状态,也导致细胞内ROS水平持续升高,从而加速了肝细胞癌的发生和进展(图1)。此外,团队还探讨了针对PIR的干预策略。结果显示,使用抗氧化剂N-乙酰半胱氨酸(NAC)、PIR抑制剂TphA以及抗IL-6的单克隆抗体等切断上述正反馈环路均能有效抑制HCC的发展。这一发现不仅为揭示HCC发展中炎症与ROS相互作用的复杂机制提供了新视角,还为针对PIR的抗HCC疗法开拓了新的方向。未来,有望通过开发更有效的PIR抑制剂,探索其在治疗HCC中的潜力。
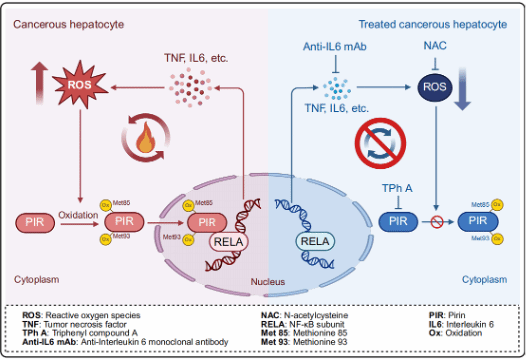
图1 PIR通过正反馈调节ROS水平和炎症反应促进HCC发生的机理
该研究的第一作者为厦门大学博士后马欢欢、博士生曹婷艳和张凤琼。厦门大学生命科学学院李勤喜教授、厦门大学附属翔安医院何伟玲教授为共同通讯作者。该研究获得了国家自然科学基金、国家重点研发计划、中国博士后基金,福建省自然科学基金、广东省基础与应用基础研究基金以及厦门大学生物医学仪器共享平台的大力支持。
全文链接:https://gut.bmj.com/cgi/content/full/gutjnl-2024-334087
(图/文 李勤喜团队)
