王耿团队揭示SEC61A1–mt-dsRNA–天然免疫轴驱动 衰老相关认知衰退的新机制
日期: 2026-02-23 访问数:衰老是认知衰退的主要诱因,但驱动衰老相关认知衰退的分子机制仍不清楚。近日,王耿教授团队在《Cell Research》杂志上发表了题为《Mitochondrial double-stranded RNA drives aging-associated cognitive decline》的研究论文。该研究首次揭示了内质网蛋白SEC61A1是调控mt-dsRNA稳态的关键因子,该蛋白在衰老大脑中特异性上调,通过增强内质网-线粒体接触(ERMCS),促进线粒体转录,导致mt-dsRNA生成与累积,激活胞质MDA5/RIG-I-MAVS天然免疫通路,从而驱动衰老相关的认知衰退。
ERMCS功能障碍已被证实与阿尔茨海默病(AD)、帕金森病(PD)和肌萎缩侧索硬化症(ALS)等多种神经退行性疾病密切相关1。有趣的是,ERMCS的变化在不同神经退行性疾病中存在差异:AD患者及大多数AD小鼠和细胞模型中,ERMCS增强2,3;与之相反,家族性PD和ALS相关的突变会导致ERMCS减弱4-7。这些差异反映了不同疾病在分子机制上的区别。与AD中ERMCS增强的现象一致,AD患者中SEC61A1表达水平、mt-dsRNA水平及RNA感知免疫信号均上调,提示mt-dsRNA介导的神经炎症可能也在AD相关的认知障碍中发挥作用。值得关注的是,SEC61A1随年龄的变化有可能是对线粒体功能衰退的一种代偿性的响应,特别是在对能量代谢高度依赖的神经元细胞里。SEC61A1的上调增强ERMCS,而ERMCS的增强又会促进线粒体DNA合成和转录8,导致mt-dsRNA水平随之上升。因此,细胞质mt-dsRNA的积累和RNA感知免疫信号的过度激活,可能只是细胞试图逆转衰老过程中线粒体功能下降的意外不良后果。
王耿教授团队长期聚焦于线粒体核酸转运与代谢研究。本研究始于一个意外发现:在探索DNA转运通道相关因子的过程中,研究人员发现内质网蛋白SEC61A1过表达可显著激活MDA5/RIG-I-MAVS信号通路。进一步分析表明,该通路的激活不依赖于SEC61A1经典的蛋白转运及质量控制功能,提示其可能通过一种全新机制发挥作用。
为明确激活dsRNA信号的内源性RNA来源,研究人员整合了免疫电镜胶体金标记、免疫荧光共聚焦成像、dsRNA特异性抗体(J2)免疫共沉淀等多层次技术,并通过线粒体DNA删除及转录抑制实验进行功能溯源。最终证实:SEC61A1过表达引发的胞质dsRNA累积与天然免疫激活,其根本来源是线粒体转录产物mt-dsRNA。该调控模式在HEK293细胞及神经元系N2a细胞中均得到验证。
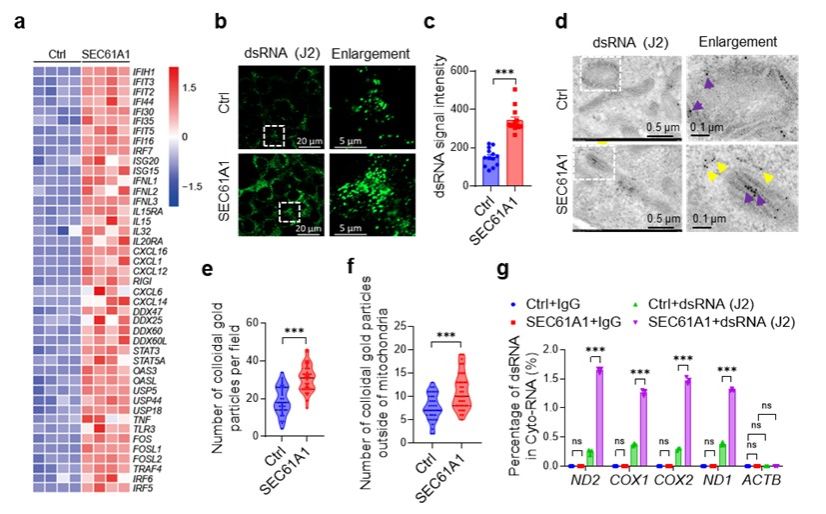
图1. SEC61A1过表达通过mt-dsRNA累积激活天然免疫
在此基础上,研究人员进一步探究SEC61A1如何调控mt-dsRNA的累积。透射电镜结果显示,SEC61A1-APEX定位于ERMCS。机制上,SEC61A1通过与线粒体蛋白RMDN3直接互作,促进ERMCS形成,进而加速线粒体DNA复制与转录,最终导致mt-dsRNA生成增多与胞质泄漏。Alphafold结构预测结合免疫共沉淀实验进一步揭示,SEC61A1的C端第471位甲硫氨酸(M471)与RMDN3通过氢键形成特异性相互作用。该位点对其功能至关重要:M471A点突变不仅破坏了SEC61A1与RMDN3的结合,还显著削弱了其对线粒体DNA合成、mt-dsRNA水平及RNA感知免疫信号通路的调控能力。
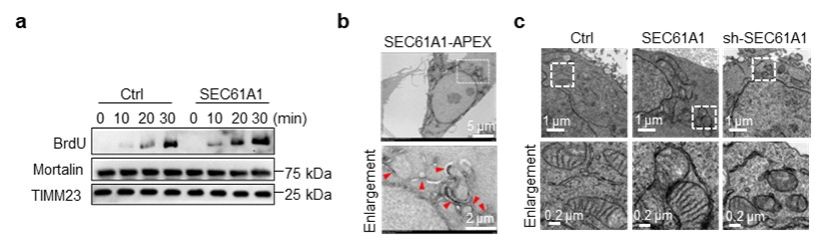
图2. SEC61A1通过促进ERMCS形成加速线粒体DNA复制与转录
研究人员发现,在自然衰老小鼠的皮层组织及AD患者皮层组织中,SEC61A1及dsRNA感受器的表达水平均显著上调。通过对AD患者现有RNA测序数据的分析,SEC61A1的表达量与简易精神状态检查(MMSE)评分呈显著负相关,提示SEC61A1的高表达可能是AD患者认知功能下降的促进因素之一。
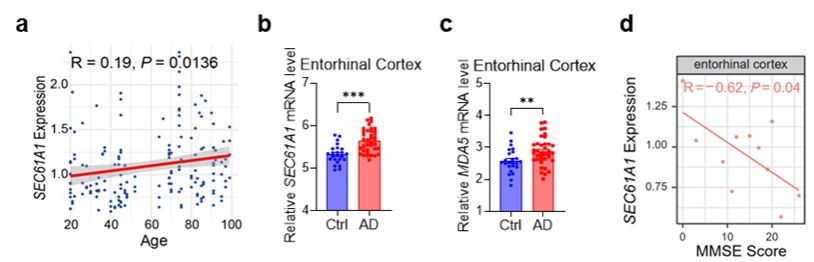
图3. 自然衰老和AD患者大脑皮层组织中SEC61A1上调和认知衰退相关
为验证这一假设,研究人员在小鼠大脑神经元中特异性过表达SEC61A1,成功模拟了衰老及AD相关的关键病理表型。分子层面检测再次证实,SEC61A1过表达激活了mt-dsRNA介导的天然免疫通路,诱发显著的神经炎症,并导致认知功能损伤。转录组与单细胞核测序进一步揭示,神经元特异性过表达SEC61A1后,神经炎症信号显著增强,神经元数量明显减少,且在神经元特异性上调基因中富集了多种神经退行性疾病相关通路。
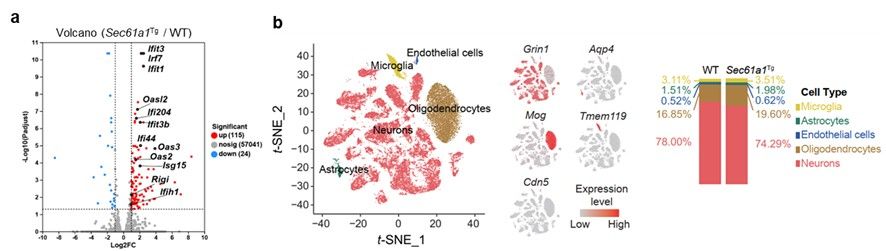
图4. 小鼠神经元中SEC61A1过表达通过激活dsRNA免疫通路诱导神经元损伤
在此基础上,研究人员通过脑立体定位注射腺相关病毒(AAV),在自然衰老小鼠中靶向敲低SEC61A1或其下游信号分子MAVS。结果显示,敲低SEC61A1或MAVS均可显著减轻神经炎症,并有效改善衰老小鼠的认知功能。
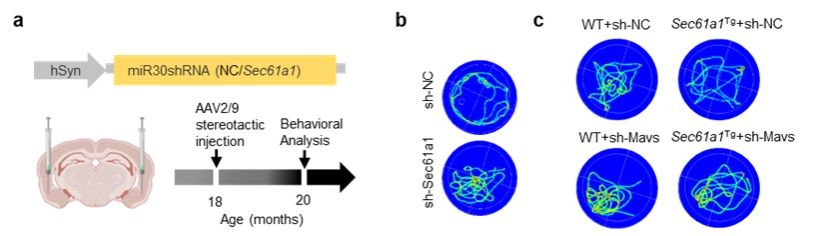
图5.神经元特异性敲低SEC61A1或MAVS改善自然衰老小鼠的认知功能
最后,研究在进化保守性层面进行了拓展验证。通过学院俞勇老师和罗津韬老师团队合作,发现在成年线虫中敲低SEC61A1的同源基因sec-61.A,同样能够抑制dsRNA水平及下游信号通路的激活,并显著延长线虫寿命。这一结果进一步支持了“SEC61A1-mt-dsRNA-天然免疫”轴在调控衰老及相关认知衰退中的核心地位及其进化保守性。
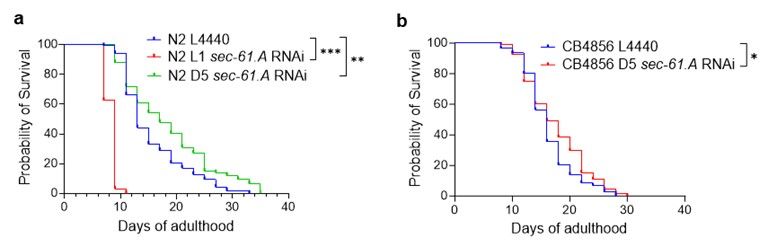
图6. 成年线虫中敲低sec-61.A显著延长线虫寿命
综上,本研究首次确立“SEC61A1–mt-dsRNA–天然免疫”轴是驱动衰老及AD相关认知衰退的关键机制,不仅揭示了炎性衰老新的起源机制,也为相关神经退行性疾病的防治提供了全新靶点与干预思路。
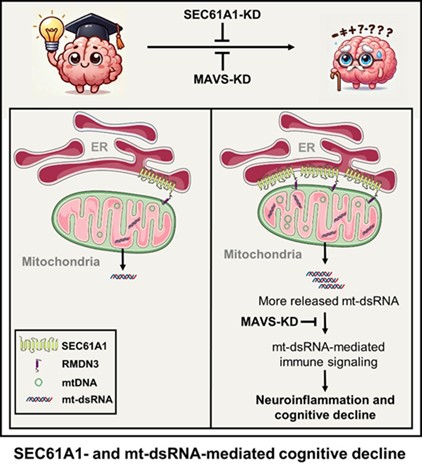
图7. “SEC61A1–mt-dsRNA–天然免疫”轴驱动衰老的模式图
厦门大学生命科学学院博士后张立孝、博士生李想、博士后罗洪笛为共同第一作者,王耿教授和张智荣博士为通讯作者。该研究得到了国家自然科学基金的资助。
全文链接:https://www.nature.com/articles/s41422-026-01224-w
(图/文 王耿组)
