尤涵教授团队揭示乳酸代谢重编程驱动LSD1乳酰化作为黑色素瘤靶向耐药的表观遗传机制
日期: 2025-03-31 访问数:黑色素瘤是威胁人类健康的最主要皮肤癌之一,与基因突变密切相关,日照损伤引起的黑色素瘤以BRAFV600E突变最为常见。BRAFV600E抑制剂和MEK抑制剂联合治疗(BRAFi/MEKi)是当前的主要靶向治疗策略。靶向药耐药问题,以及耐药肿瘤常伴随免疫抑制微环境的形成,导致免疫治疗失败,是临床治疗黑色素瘤的严峻挑战。在临床上,靶向治疗耐药黑色素瘤活检中经常发现葡萄糖代谢恢复的现象。但是,恢复的糖酵解如何控制BRAFi/MEKi获得性耐药的出现,尤其是绕过BRAF/MEK通路的内在机制,目前尚不明确。近年来,乳酸介导的表观遗传修饰功能备受关注——其介导的组蛋白赖氨酸乳酰化修饰可重塑基因转录景观,在肿瘤进展、免疫逃逸等过程中发挥核心作用。乳酸在靶向药耐药进程中的动态改变如何影响表观遗传级联反应及其对靶向-免疫双耐药的影响知之甚少。
2025年3月24日,尤涵教授团队在Developmental Cell杂志在线发表题为“Lactylation of LSD1 is an acquired epigenetic vulnerability of BRAFi/MEKi-resistant melanoma”的研究论文。该研究首次揭示靶向药耐受黑色素瘤中乳酸驱动的LSD1乳酰化修饰通过抑制铁死亡维持耐药细胞生存的机制。提出LSD1抑制剂通过触发耐药细胞铁死亡,重塑肿瘤免疫微环境,增敏PD-1抑制剂的全新策略,为克服靶向药耐受提供精准靶点。

本研究发现靶向药耐受黑色素瘤细胞中重新积累的乳酸诱导了LSD1 K503位点的乳酰化,通过表观遗传重编程选择性地驱动细胞存活。其机制包括:1.耐药细胞中LSD1的乳酰化修饰促进其与FosL1的结合,阻止LSD1被E3连接酶TRIM21结合并降解;2.耐药细胞中FosL1自身乙酰化修饰水平降低,促进其染色质结合能力显著增强,FosL1与乳酰化的LSD1共同协调基因转录,通过干扰铁死亡关键调控因子TFRC转录维持耐药细胞存活。
利用PDX和小鼠黑色素瘤模型,本研究发现LSD1抑制剂(LSD1i)通过激活铁死亡,选择性抑制靶向药耐受黑色素瘤的生长。更重要的是,LSD1i诱导的铁死亡可重塑免疫微环境,促进M1型巨噬细胞以及CD8+ T细胞的浸润,恢复靶向治疗耐受BRAFV600E黑色素瘤对免疫检查点阻断(Immune Checkpoint Blockade, ICB)的响应。
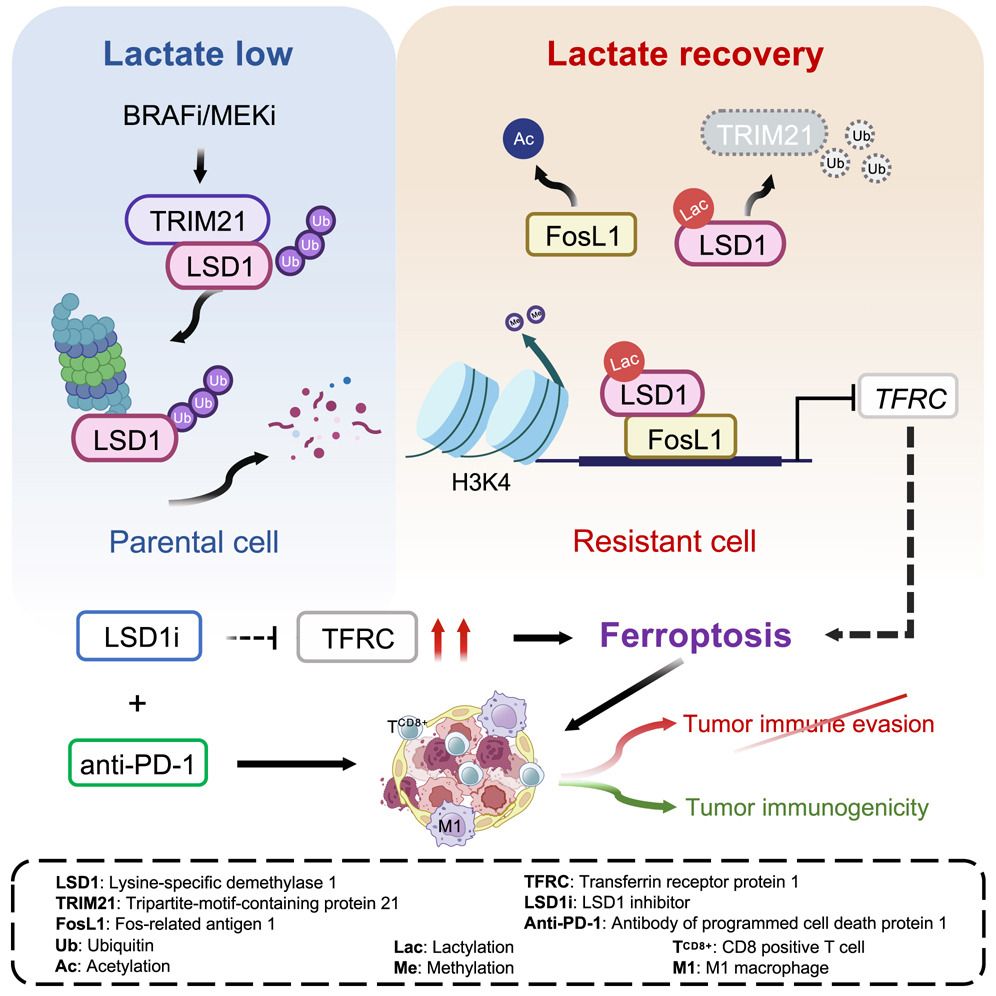
该研究结果揭示了代谢重编程诱导的表观遗传修饰重编程作为靶向药耐受黑色素瘤旁路抵抗机制的关键作用,提出靶向LSD1激活铁死亡并协同免疫治疗的新策略,为黑色素瘤精准治疗提供理论依据。
该研究由厦门大学博士研究生李瑷存与江南大学附属医院龚志成助理研究员完成。尤涵教授与空军军医大学叶菁教授为共同通讯作者,该研究得到国家自然科学基金委资助。
原文链接:https://doi.org/10.1016/j.devcel.2025.02.016
(文/图 尤涵教授团队)
